
联系我们
地址: 安徽省合肥市高新区望江西路5089号
邮编: 230026
电话: 0551-62391679
邮箱: iai@iai.ustc.edu.cn
顶刊再+1!我院成果登上《Science》:解决神经突触传递机制延续半个世纪的关键争议
文章来源:本站原创 发布时间:2025-10-22 09:09:12 文章作者:本站编辑
作为关键参与方和核心支撑平台,合肥综合性国家科学中心人工智能研究院(以下简称“人工智能研究院”)在人工智能与神经突触传递领域取得重大技术突破,相关成果发表于国际顶尖学术期刊《科学》(Science)。此项研究由我院“介观神经图谱解析”科研团队成功研发出毫秒级时间分辨原位冷冻电镜成像技术,标志着我院在此前沿交叉领域已达到国际领先地位。
大脑作为接收、加工、处理外界信息的主体,其功能的实现依赖于数千亿个神经元之间高效、精准的突触传递。突触囊泡释放神经递质介导了神经元之间的信号传递。自1970年代初以来,科学界围绕囊泡释放机制逐渐形成了两种对立的模型:全融合(Full-collapse)和亲吻-逃逸(Kiss-and-run)。由于囊泡释放过程发生在毫秒时间尺度、结构变化处于纳米空间尺度,传统技术很难以纳米分辨率捕捉其瞬时动态,因此这一谜题悬而未解,困扰学界长达半个世纪之久。
为攻克此难题,人工智能研究院毕国强教授、刘北明教授领导的科研团队,联合中国科学技术大学、中国科学院深圳先进技术研究院、美国加州大学洛杉矶分校等单位,通过自主研发的毫秒级时间分辨原位冷冻电镜成像技术,破解了神经信息传递过程中,突触囊泡释放与快速回收的生物物理过程——“亲吻-收缩-逃逸/融合”(Kiss-Shrink-Run/Collapse)(图1)。这一成果统一了半个世纪以来学界关于突触囊泡释放与回收机制的两个争议模型,为理解神经信号传递、神经可塑性及相关脑疾病机理提供全新视角。相关成果于北京时间10月17日发表在《科学》期刊。
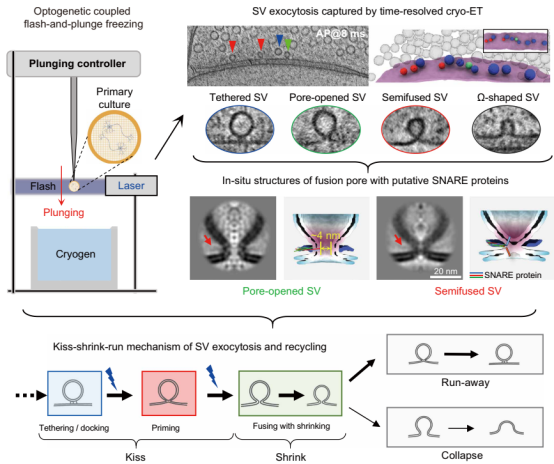
图1. 时间分辨冷冻电镜技术解析突触囊泡释放与回收动态过程
冷冻电镜断层三维成像技术(Cryo-electron tomography, cryo-ET)能够对生理状态下的细胞在原位实现纳米精度的成像并能够获得细胞的分子水平结构数据,已成为在细胞原位解析蛋白质等生物大分子结构及其三维空间分布的强有力工具。2010年起,团队就致力于将cryo-ET成像应用于神经突触的结构与功能研究中。在该研究中,团队首次在神经突触的突触前区域中观测到一类直径约为29纳米的“小囊泡”(正常突触囊泡直径约为42纳米左右),并推测其为囊泡释放的中间状态(图2)。

图2. 冷冻电镜原位成像实现对囊泡三维形态的分割与定量表征
为“看清”突触囊泡传递信息的动态过程,研究团队将光遗传学刺激与投入式冷冻技术进行耦合,开发出毫秒级时间分辨的冷冻电镜制样技术,通过光刺激诱导神经元传递电信号,在信号发出后的4毫秒至300毫秒之间的不同瞬间,对细胞进行快速冷冻“定格”,精准捕捉囊泡释放的瞬时状态,并由此获得上千套高分辨率的神经突触三维重构数据。进一步结合图像处理技术,研究人员清晰地分辨出囊泡与细胞膜的半融合结构、囊泡与细胞膜形成的狭小融合孔、以及介导囊泡融合的蛋白复合物,明确了这些囊泡是处于释放的中间状态,并进一步解析出不同形态的突触囊泡数量随时间的变化规律(图3)。
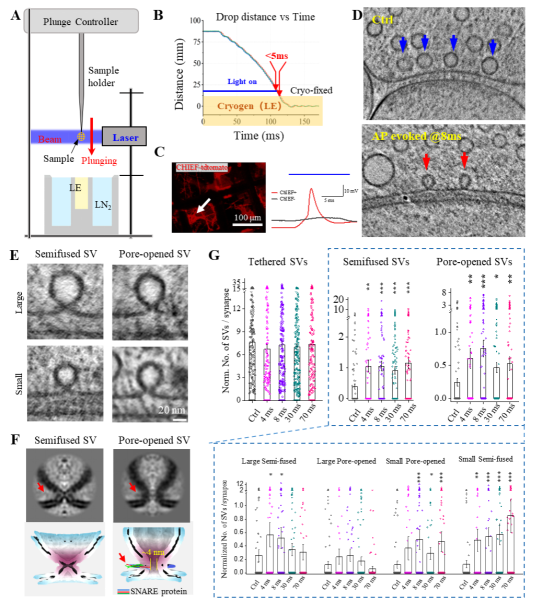
图3. 时间分辨冷冻电镜技术捕捉突触囊泡释放的动态过程
基于此,研究团队清晰地揭示了突触囊泡释放与快速回收的完整过程,并提出“亲吻-收缩-逃逸/融合” (Kiss-Shrink-Run/Collapse)全新的理论模型:当动作电位触发后4毫秒内,囊泡先与突触前膜“亲吻”(kiss)形成约4纳米的融合孔,随后,快速收缩至表面积减半的小囊泡(shrink),最终,大部分小囊泡在70毫秒内开始以“逃逸”(Run)方式离开,少部分则与突触前膜“全融合”(Collapse)(图4)。
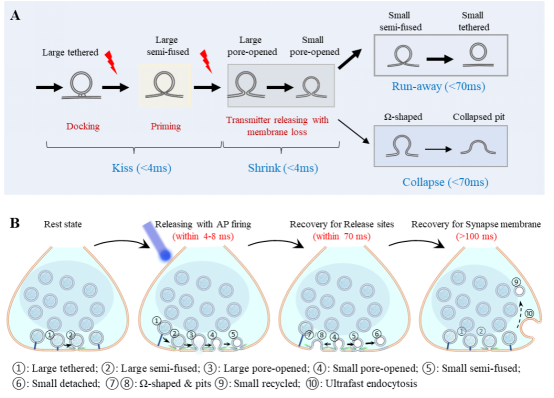
图4.突触囊泡释放与快速回收
这一研究首次发现了细胞原位突触囊泡释放时伴随着膜丢失进而变小的现象(“收缩”,shrink),并对囊泡释放前后极短的时间内的动态变化进行了严格的量化分析,同时对其中的分子机制进行了初步探究,更新了传统认知:“亲吻-收缩-逃逸”是囊泡释放的主要途径,传统对立的全融合与亲吻-逃逸模式,实为统一流程的不同结局,合理解释了神经突触实现高效、高保真信号传递的结构基础。这项工作的创新性与影响力获得了《科学》期刊审稿人的高度认可,称“这是一项卓越的研究,提供了富有洞察力的视角”。
这一成果破解了困扰神经科学领域半个世纪的谜题,揭示了突触传递的核心生物物理过程,为理解神经信息加工、脑认知功能机制提供了重要理论基石,为开发新一代人工智能模型和阐明神经精神疾病的病理提供了全新的视角。

图5. 导师与团队成员讨论数据分析
中国科大与人工智能研究院双聘毕国强教授和刘北明教授、中国科大陶长路特任副研究员、美国加州大学洛杉矶分校周正洪(Z. Hong Zhou)教授为本论文的共同通讯作者。中国科大特任副研究员陶长路、博士生田崇礼(现为中国科学院深圳先进院博士后)、博士生刘云涛(现为加州大学洛杉矶分校博士后)、博士生卢振航为该论文的共同第一作者。





